編入試験 よく出る! 人名反応
編入試験の化学では人名反応のように少し難しい反応がいくつか出てきます。
ただ、人名反応はマイナーなものからメジャーなものまでほんとに数が多いので今回の記事では実際に過去問で出題されたことのある人名反応について記事にしてみました。
反応の説明では反応の基礎的な説明から少し応用的な話(特に説明の後半で多い)も含めています。なので、まずは説明の前半だけを理解し、後半もぜひ読んでみてください。
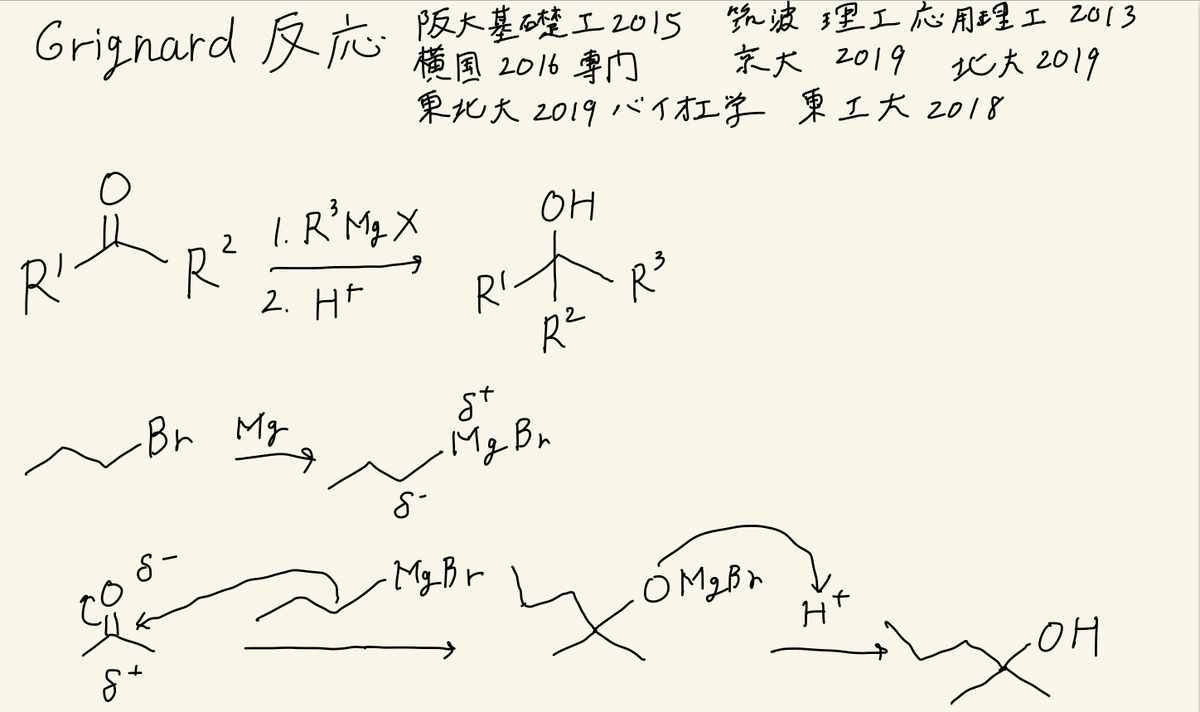
人名反応の王道中の王道、Grignard(グリニャール)反応
編入試験の中では一番頻出頻度が多い人名反応がこのGrignard反応でした。この反応はケトンまたはアルデヒドをアルコールに変換する反応です。まず、ハロゲン化アルキルをマグネシウムと反応させ、Grignard試薬を合成する。次にGrignard試薬がケトン、またはアルデヒドのカルボニル炭素に対して求核付加反応を起こします。

この反応は反応機構がシンプルで分かりやすいので編入試験では出題されることも多い反応です。まず、塩基である水素化ナトリウムによってアルコキシド中間が生じ、ハロゲン化アルキルに対してSN2反応でエーテルを合成する。SN2反応では非プロトン性の極性溶媒を用いると、求核剤の基底状態のエネルギーを上げるため、反応性が高くなります。

芳香環との反応では一番有名かも?Friedel-Crafts(フリーデルクラフツ)反応
この反応は上がFriedel-Craftsアシル化反応、下がFriedel-Craftsアルキル化反応と呼ばれます。どちらも反応機構は同じです。まずLewis酸である塩化アルミニウムが触媒として塩化アシル、塩化アルキルから塩素を抜き取ります。これによって活性化されたアシル化剤、アルキル化剤は芳香環に対して求核付加反応が起こります。最後に水素がプロトンとして脱離して反応が完成です。アシル化とアルキル化での違いはそのあとです。アシル基は電子吸引性なので、芳香環が置換された後、2つ目、3つ目の求核付加反応の反応速度は遅くなります。一方、アルキル基は電子供与基であるため、1つ目の置換が起こってから、2つ目、3つ目の求核付加反応が進行します。このため、Fridel-Craftsアルキル化は生成物が混合物となりやすい欠点があります(ただし、立体障害の大きいアルキル基では次の置換は抑制されます)。

アミドからアミンに、Hoffman転移
この反応はアミドから炭素数が一つ減ったアミンを合成する反応です。塩基によるプロトンの引き抜きから始まり、脱炭酸に伴ってアミンに変換されます。

Clemmensenの相方、Wolff-Kishner還元
この反応で出てくるアミノ基がH2NNH2はヒドラジンといい、ケトン、アルデヒドに対する反応ではよく出てきます。この反応は後で説明するClemmensen還元とは対照的に塩基条件下で反応が進行するというのが特徴の一つです。

Wolff-Kishner還元の相方、Clemmensen還元
この反応はさきほどのWolff-Kishner反応と違い、酸性条件下で反応が進行します。ただこの反応では、水銀を必要としているので、もしかしたら上の反応機構を改良した優れた方法がすでに開発されているかもしれません(編入試験では上のように水銀を使ったものが出題されてましたが)

エステルがないならケトンから作ればいいじゃない、Baeyer-Villiger酸化
この反応は過酸という通常のカルボン酸よりも酸素の数が一つ多い分子を使ってケトンからエステルを合成します。今回の反応機構ではm-クロロ過安息香酸が過酸として使われています。今回のように環状のケトンに対してBaeyer-Villiger反応を起こすと、ラクトン(環状エステルのこと)が合成できます。少し脱線しますが、実はこの反応を微生物(酵素)の力を使ってやってみようという研究もあり、印象的でした。

二つのエステルを合わせて、Claisen縮合
この反応はアルドール縮合と同じような(というかほぼ完全に同じ)反応機構で進行するので、アルドール縮合を先に覚えていると簡単に反応機構が覚えられてしまいます。
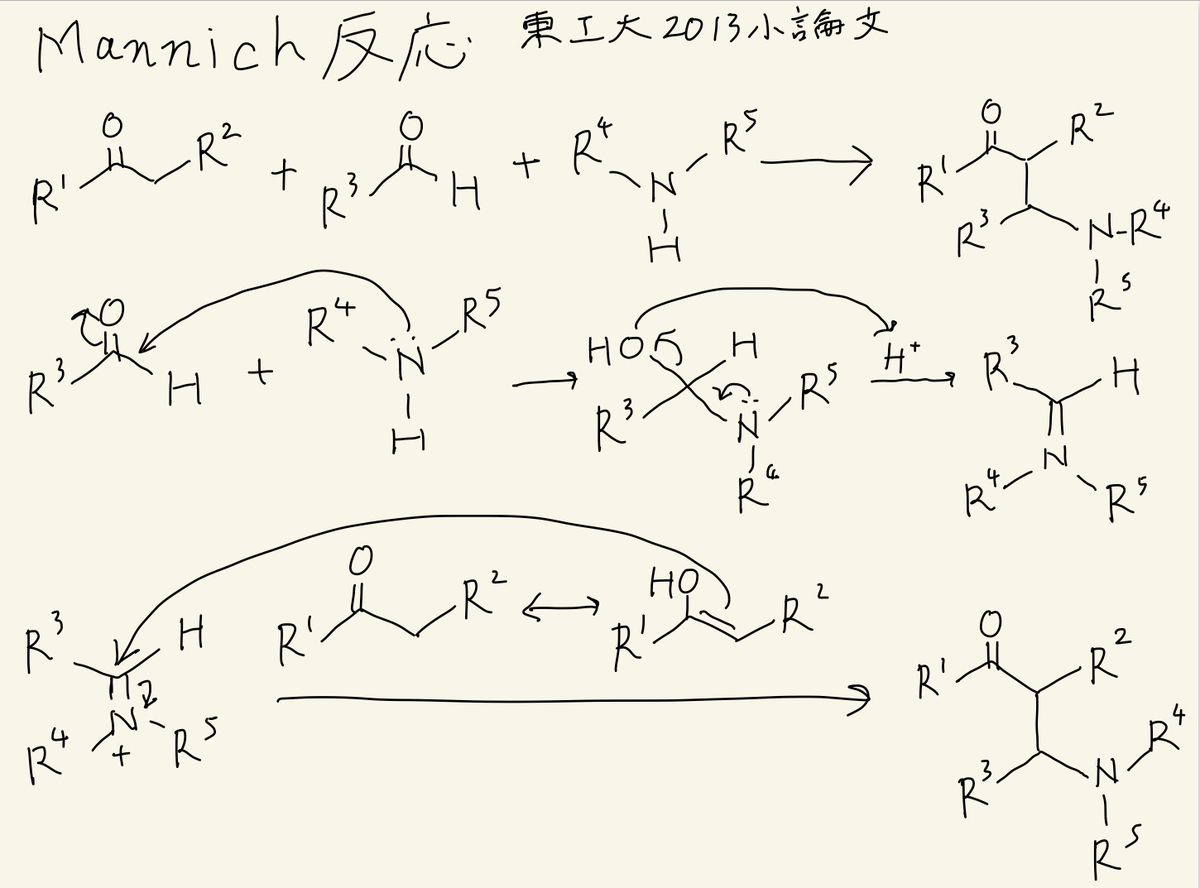
H1拮抗薬での中心的な反応、Mannich(マンニッヒ)反応
花粉症の人だと聞いたことがあるかもしれない抗ヒスタミン薬という薬の合成でよく出てくるのがこのMannich反応です。アルデヒド、二級、または一級アミン、α水素を持ったケトンによって進行します。α水素というのはカルボニル炭素の隣の炭素に結合した水素のことで、さらにその隣をβ水素、さらに隣をγ水素・・・と呼びます。

割と珍しい環の形成方法、D-els-Alder(ディールス・アルダー)反応
この反応は僕が初めて知った人名反応なので割と思い入れがあります。この反応は今までのように分子や官能基の極性による反応ではなく、ペリ環状反応と呼ばれる種類のはんのうです。共役ジエンとアルケンの反応によって六員環のアルケンが合成されます。また、その関係性は立体特異的でシスのアルケンではシスの六員環が、トランスのアルケンではトランスの六員環が形成されます。たしか化学オリンピックの予選でもこの問題がでたことがありました。

アミンからアルケンに、Hoffman脱離
この反応はアミンに過剰量のヨードメタンを加え、アルケンへと変換します。ここで使われる酸化銀は四級アンモニウム塩の対イオンをヨウ化物イオンからOH-にするために加えられています。




